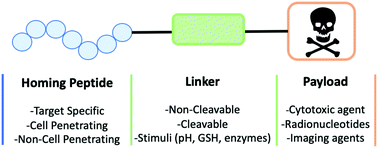
Unatoč stalnom napretku u terapiji konjugatima antitijela i lijeka (ADC), nekoliko izazova ostaje. Na primjer, složena struktura ADC dovodi do visokih troškova proizvodnje i dugog poluživota, što povećava sustavnu toksičnost zbog produljene izloženosti u plazmi. Posljedično, konjugati peptida i lijeka (PDC) pojavili su se kao alternativa koja obećava. PDC se sastoje od tri komponente: peptida za samonavođenje, povezivača i lijeka korisnog opterećenja. Koristeći visok afinitet peptida za samonavođenje za površinske receptore tumora, PDC-ovi isporučuju korisni lijek izravno na cilj.

Oblici PDC nosivosti
PDC mogu nositi različite oblike korisnog tereta. To mogu biti konvencionalni lijekovi za kemoterapiju poput paklitaksela ili gemcitabina. Radioaktivni izotopi također se koriste za preciznu dijagnozu bolesti i ciljanu radioterapiju. Dijagnostički izotopi uključuju fluor-18 (18F), bakar-64 (64Cu), galij-68 (68Ga) i jod-123 (123I). Ovi izotopi, konjugirani s ciljanim peptidima, vežu se na receptore tumorskih stanica, omogućujući preciznu lokalizaciju malignih tkiva putem detekcije pozitrona koje oslobađaju izotopi. Kada su ciljani peptidi povezani s radioaktivnim izotopima kao što su indij-111 (111In), itrij-90 (90Y) i lutecij-177 (177Lu), PDC-ovi funkcioniraju kao sredstva ciljane radioterapije. Ostala korisna opterećenja za PDC uključuju proteine, antitijela, peptide i nukleinske kiseline.

Prednosti PDC-a
PDC-ovi nude sličnosti s ADC-ovima, ali nadilaze neka njihova ograničenja. U usporedbi s ADC-ima, PDC-i imaju manju molekularnu težinu, bolju penetraciju u tkivo i manju ili nikakvu imunogenost. Nadalje, PDC-ove je lakše sintetizirati, pročistiti i identificirati, što rezultira nižim troškovima proizvodnje. S napretkom u tehnologiji ciklizacije, tehnologiji prikaza faga i tehnologiji prikaza mRNA za ciljani odabir peptida, razvoj lijekova PDC je ubrzan. PDC-ovi su spremni postati sljedeća generacija ciljanih lijekova nakon ciljanih lijekova na male molekule, lijekova s antitijelima i ADC-ova.
Farmakokinetičke karakteristike PDC-a
ApsorpcijaPDC imaju relativno veliku molekularnu težinu i slabu propusnost u usporedbi s tradicionalnim malim molekulama. Zbog nestabilnosti njihovih peptida u gastrointestinalnom traktu, trenutni PDC na tržištu iu kliničkim stadijima primjenjuju se intravenozno, zaobilazeći proces apsorpcije. Također se mogu primijeniti supkutano ili intramuskularno, ulazeći u krvotok ili limfni sustav. Značajan nedostatak PDC-a kao lijekova je njihova nestabilnost i kratak poluživot in vivo, budući da se peptidi brzo razgrađuju proteazama i lako se uklanjaju putem bubrega. Ovo je posebno problematično u liječenju solidnog tumora, gdje je potrebna produžena cirkulacija za adekvatnu penetraciju tumorskog tkiva. Modificiranje peptida za povećanje stabilnosti i produljenje poluživota ključna je strategija.
DistribucijaPDC peptidi su kategorizirani u dvije vrste: Peptidi koji ciljaju na stanicu (CTP) i Peptidi koji prodiru u stanicu (CPP). Zbog niske specifičnosti CPP-ova za stanice, oni se općenito ne koriste kao peptidi za samonavođenje u PDC-ima. PDC-i ciljaju tumore na dva načina: 1) PDC-i se vežu za prekomjerno izražene receptore na površini tumorskih stanica, ulaze u stanice putem endocitoze i oslobađaju toksine u lizosomima; 2) PDC otpuštaju toksine u okolinu tumora, koji zatim ulaze i ubijaju tumorske stanice.
MetabolizamPDC se metaboliziraju in vivo putem tri glavna puta:
- Ciljno posredovana dispozicija lijeka (TMDD): TMDD je specifičan put eliminacije. PDC se vežu na receptore na ciljnim stanicama, internaliziraju se i razgrađuju u aminokiseline i peptide u lizosomima. Međutim, broj ciljeva na površini stanica obično je ograničen, što čini TMDD zasićenim i dovodi do nelinearne farmakokinetike.
- Nespecifični metabolizam: Neciljani procesi poput proteolize i nespecifične pinocitoze mogu otpustiti male molekule citotoksina na neželjenim mjestima, uzrokujući nuspojave izvan cilja.
- Imunogenost: PDC mogu potaknuti imunogenost, potičući proizvodnju antitijela protiv lijekova (ADA), koja neutraliziraju lijek i stvaraju komplekse koje imunološki sustav čisti. Važno je napomenuti da imunogenost ili ADA odgovori opaženi kod pretkliničkih životinja ne predviđaju ljudske ADA odgovore.
IzlučivanjePDC, molekularne težine puno manje od praga bubrežne filtracije (60 kDa), brzo se uklanjaju putem bubrega, sprječavajući učinkovito nakupljanje citotoksina u tumorima. Stoga su potrebne modifikacije ili kemijske izmjene peptida za samonavođenje PDC-a kako bi se povećala stabilnost i produžio poluživot. Bubrežno izlučivanje može biti primarni put uklanjanja nekih peptida ili PDC lijekova. U takvim slučajevima, ključno je uzeti u obzir da se brzina klirensa izračunata iz analize bez odjeljaka (NCA) nakon IV primjene treba odnositi na brzinu glomerularne filtracije lijeka, a ne na protok krvi u jetri.
Strategije farmakokinetičke studije za PDC
PDC-ovi inherentno koriste strategije ciljanja za isporuku lijekova, kombinirajući karakteristike lijekova velikih i malih molekula. Zbog njihove relativne nestabilnosti i problema s ciljanjem, potencijalna toksičnost korisnog tereta zahtijeva posebnu pozornost. U fazi probira lijekova, studije DMPK usmjerene su na poboljšanje stabilnosti peptida i PDC-a u punoj krvi, plazmi i bubrežnom homogenatu, dok se nastavlja optimizirati struktura PDC-a putem in vitro i in vivo identifikacije metabolita kako bi se poboljšala stabilnost i poluživot. Preporuča se provesti studije distribucije tkiva na glodavcima u ranoj fazi projekta kako bi se procijenila potencijalna toksičnost korisnog tereta za različite organe.
U fazi kliničkog kandidata potrebno je identificirati odgovarajuće in vitro modele kako bi se procijenilo i potvrdilo in vivo oslobađanje korisnog tereta. Pokusi in vivo trebali bi istodobno mjeriti koncentraciju PDC-a i korisnog tereta u krvi. U uvjetima ponovljenog doziranja, preporučljivo je pratiti učinke ADA. Provođenje eksperimenata distribucije tkiva u vrstama PD-a neophodno je za procjenu sposobnosti ciljanja PDC-a.
Zaključak i perspektiva
Unatoč velikom iskustvu u razvoju lijekova ADC, razvoj lijekova PDC nije jednostavan put, već je put ispunjen i prilikama i izazovima. U usporedbi s ADC-ima, tkivna specifičnost i ciljanje tumora peptida donekle su inferiorni, što predstavlja značajne izazove za odabir ciljanih peptida. Dodatno, zbog slabe stabilnosti peptida, oralna primjena predstavlja znatnu poteškoću. PDC-ovi se također suočavaju s analitičkim izazovima i potencijalnim neciljanim učincima.
Dizajn PDC lijekova integrira prednosti ciljanja peptida i raznih vrsta lijekova. Nedavna regulatorna odobrenja radionuklidnih terapeutskih lijekova i dijagnostičkih sredstava naglašavaju potencijal ovih lijekova. Ohrabrujući klinički rezultati iz kliničkih procesa koji su u tijeku dodatno naglašavaju njihovo obećanje. Uz konjugaciju različitih molekularnih entiteta i ciljanih peptida, razvoj PDC lijekova ima veliki potencijal za budućnost.